Si un gen alterado causa cáncer y crea una proteína para el cáncer, ¿se puede aislar la nueva proteína de alguna manera?
Anónimo
En la pregunta del título anterior, ¿no se puede aislar la proteína alterada (para separarla de otras proteínas) de alguna manera? ¿No hay nada que pueda unirse a las proteínas específicas del cáncer que no se una a otras proteínas?
Respuestas (1)
MattDMo
Por cómo leí su pregunta, se pregunta si existe alguna tecnología para aislar de alguna manera las proteínas oncogénicas dentro de la célula para que no causen daño, ¿es correcto?
La respuesta es algo complicada, ya que depende de la proteína. Sin embargo, primero debe comprender que el cáncer es una enfermedad muy compleja y que el cáncer no es causado por una sola mutación. La hipótesis de los "golpes múltiples" o de Knudson establece esencialmente que una célula progresa de una célula normal a una cancerosa, acumulando múltiples mutaciones en el camino. En casi todos los casos, se necesitan al menos dos mutaciones específicas: la activación constitutiva de un protooncogén , un grupo de proteínas responsables del crecimiento y la proliferación celular, y la eliminación o inactivación de uno o más genes supresores de tumores., que se utilizan para mantener bajo control el crecimiento y la proliferación. De esta manera, tiene un conductor de tumor (a menudo se trata de una sola proteína, como un receptor de factor de crecimiento ) que "dirige" el proceso oncogénico , sin "freno" ni regulación.
Como dije, las mutaciones en los genes supresores de tumores generalmente dan como resultado cambios en la pérdida de función, o la eliminación/desactivación completa del gen, por lo que "aislar" estas proteínas en la célula no serviría de mucho. El objetivo de muchas terapias tumorales es regular a la baja, inhibir, destruir o eliminar de otro modo la función de la proteína que impulsa el crecimiento y la proliferación descontrolados de las células, formando tumores y metástasis . Si tenemos suerte, el conductor del tumor es una proteína que contiene un dominio extracelular (como un receptor de la superficie celular) que se puede identificar y atacar desde el exterior de la célula. Una vez que esto ha ocurrido, los científicos y médicos pueden usar anticuerpos monoclonales derivados especialmentepara apuntar y matar las células que contienen estas proteínas:
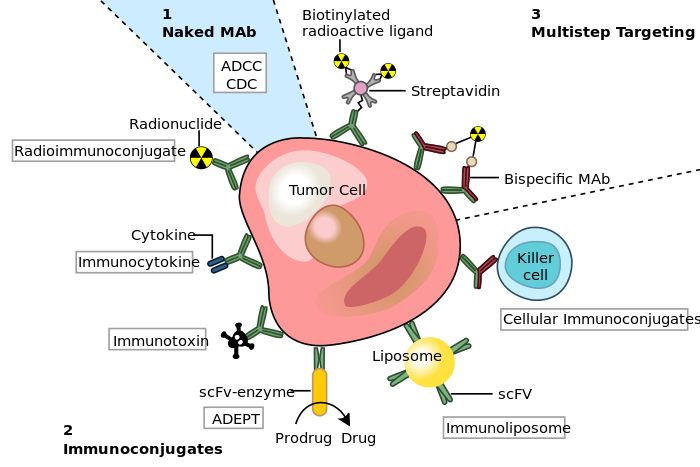
Anticuerpos monoclonales para el cáncer. ADEPT, terapia con profármacos enzimáticos dirigidos por anticuerpos; ADCC, citotoxicidad mediada por células dependiente de anticuerpos; CDC, citotoxicidad dependiente del complemento; MAb, anticuerpo monoclonal; scFv, fragmento variable monocatenario.
De WikiMedia Commons , lanzado al dominio público.
Hay varias formas en que se pueden eliminar las células cancerosas, desde la administración de radiación u otros compuestos citotóxicos hasta la atracción de células asesinas del sistema inmunitario y la activación del sistema del complemento . Sin embargo, todo esto depende de la presencia en la superficie de biomarcadores para las células cancerosas, a fin de evitar la destrucción no específica o los efectos fuera del objetivo.
La razón por la que se pone tanto énfasis en matar las células cancerosas en lugar de tratar de aislar a los "chicos malos" dentro de las células es que para cuando la célula se vuelve cancerosa, ya ha acumulado tantas mutaciones que a) la célula no es t realmente vale la pena salvar, yb ) se necesitaría un esfuerzo extraordinario para juntar todas las proteínas mutadas y dejar que las proteínas no afectadas o de "tipo salvaje" hicieran su trabajo.
Puede recordar que cada gen que tenemos (excepto algunos en los cromosomas X e Y) está presente por duplicado, una copia de nuestra madre y otra de nuestro padre. Las mutaciones iniciales que inician la progresión hacia el estado totalmente canceroso pueden afectar al principio solo a una de esas dos copias del gen, dejando una versión funcional por un tiempo. Sin embargo, a medida que avanza la oncogénesis y se inactivan más y más proteínas reguladoras, aumenta el daño cromosómico y, con frecuencia, la copia "normal" superviviente se muta o se destruye por completo. Una vez que esto ocurre, incluso si pudieras aislar las proteínas que se comportan mal, no quedarían proteínas buenas para hacer el trabajo de la célula. Por lo tanto, matar es realmente la única opción.
Espero haber cubierto lo que le interesaba. Por favor, hágamelo saber si no entiende algo de esto, o siempre puede hacer una nueva pregunta .
usuario6116
¿Cómo se relacionan las mutaciones y la síntesis de proteínas con el cáncer?
¿Cómo se miden las tasas de error de la ADN polimerasa?
¿Se requiere resolver el cáncer para evitar el envejecimiento?
¿Hasta qué punto es posible entender si una bacteria puede producir una proteína? (¡solo en silico!)
Significado de 'motivo' en biología molecular
Dificultad para encontrar fármacos inhibidores de proteínas
¿Cuál es el código del sitio de unión reconocido por las partes del spliceosoma?
¿Puede el dogma central funcionar a la inversa?
Pros y contras de la estructura de aminoácidos frente a las secuencias de ADN para la comparación evolutiva [cerrado]
¿No es estrictamente imposible la inmortalidad biológica?
MattDMo
usuario6116
MattDMo
MattDMo
usuario6116
MattDMo
usuario6116